【适应症】
本品单药适用于既往接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗血管内皮生长因子(VEGF)治疗、抗表皮生长因子受体(EGFR)治疗(RAS野生型)的转移性结直肠癌(mCRC)患者。
【推荐剂量】
每次 5mg(1 粒,每粒含 5mg 呋喹替尼),每日 1 次;连续服药 3 周,随后停药 1 周(每 4 周为一个治疗周期)。
【不良反应】
最常见的不良反应(发生率≥20%)是高血压、掌跖红肿、蛋白尿、发声困难、腹痛、腹泻和乏力。
【药理作用】
呋喹替尼是一具有高度选择性的肿瘤血管生成抑制剂,其主要作用靶点是 VEGFR 激酶家族 VEGFR1,2 及 3。呋喹替尼在分子水平可抑制 VEGFR 激酶的活性;在细胞水平上可抑制 VEGFR2/3 的磷酸化,抑制内皮细胞的增殖及管腔形成;在组织水平上,呋喹替尼可明显抑制鸡胚绒毛尿囊膜模型新生微血管的形成;在整体动物水平上,呋喹替尼口服后可抑制VEGFR2/3 磷酸化,抑制肿瘤血管生成,从而抑制肿瘤生长。在整体动物上,呋喹替尼采用一日一次给药,对结直肠癌以及其它多种类型肿瘤模型的生长均显示强效且剂量依赖性的抑制效应,在敏感模型上发现肿瘤缩小和消退。
【贮藏】
密封,30°C 以下保存
【有效期】
美版为24个月
国内版为36个月
【使用方法】
本品需在有经验的抗肿瘤医生指导下使用。
推荐剂量和服用方法
每次 5mg(1 粒,每粒含 5mg 呋喹替尼),每日 1 次;连续服药 3 周,随后停药 1 周(每 4 周为一个治疗周期)。
本品可与食物同服或空腹口服,需整粒吞服。建议每日同一时段服药。
治疗时间
持续按治疗周期服药,直至疾病进展或出现不可耐受的毒性。
【剂量调整】
表1提供了针对不良反应的推荐剂量减少。
表 1:FRUZAQLA 的推荐剂量减少

对于无法耐受每日一次口服 3 mg 的患者,永久停用 FRUZAQLA。
表2提供了针对不良反应的推荐剂量调整。
表 2:FRUZAQLA 的推荐剂量调整
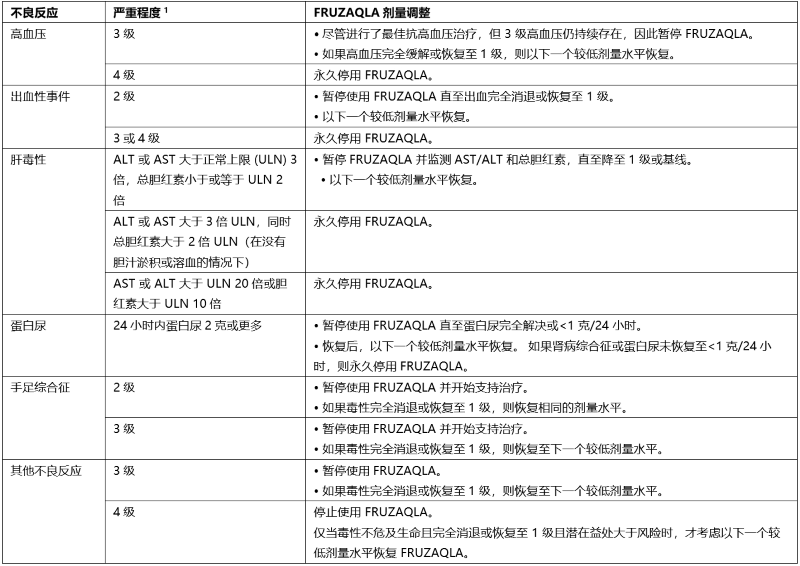
1 严重程度由美国国家癌症研究所 (NCI) 不良事件通用术语标准 (CTCAE) 5.0 版定义。
【延迟或遗漏给药】
如果服药后患者呕吐,无需补服;漏服剂量,不应在次日加服,应按常规服用下一次处方剂量。
【过量处理】
目前尚不清楚过量服用本品可能产生的危害。在本品早期剂量探索的临床研究中,部分实体肿瘤患者服用至每天 6mg 呋喹替尼,在该剂量下观察到的剂量限制性毒性为手足皮肤
反应和乏力。在转移性结直肠癌的 II、III 期临床研究中,仅发现个别患者有单次的药物过量(最高剂量为 10mg/天),但未出现重要的异常临床表现。本品用药过量没有特定的解毒药。如疑似药物过量,应立即停用本品,对患者进行密切观察,必要时采取最佳支持治疗。
【不良反应】
最常见的不良反应(发生率≥20%)是高血压、掌跖红肿、蛋白尿、发声困难、腹痛、腹泻和乏力。
【注意事项】
• 高血压:治疗前控制血压并在治疗期间监测。 如有必要,使用抗高血压药物进行管理并调整 FRUZAQLA 的剂量。 根据高血压的严重程度暂停、减少剂量或永久停药。
• 出血事件:密切监测有出血风险的患者。 根据出血的严重程度和持续情况,暂停、减少剂量或永久停用 FRUZAQLA。
• 感染:治疗期间监测感染情况,并在活动性感染期间停用FRUZAQLA。 患有活动性感染的患者请勿开始 FRUZAQLA。
• 胃肠道(GI) 穿孔:定期监测胃肠道穿孔。 对于发生胃肠道穿孔或瘘管的患者,永久终止 FRUZAQLA。 (5.4)
• 肝毒性:在开始FRUZAQLA 之前和治疗期间定期监测肝功能。 根据严重程度暂停、减少剂量或永久停药。
• 蛋白尿:监测尿蛋白。 因肾病综合征终止 FRUZAQLA 。
• 手足综合征:根据严重程度暂停FRUZAQLA。
• 可逆性后部白质脑病综合征(PRES):如果怀疑并通过磁共振成像(MRI) 确诊为PRES,请立即停用FRUZAQLA。
• 伤口愈合受损:在大手术前停用FRUZAQLA 2 周。 大手术后至少 2 周内以及伤口充分愈合之前不要给药。 伤口愈合并发症解决后恢复 FRUZAQLA 的安全性尚未确定。
• 动脉血栓栓塞事件:近期有血栓栓塞事件史的患者应仔细考虑开始FRUZAQLA。 发生动脉血栓栓塞的患者停用 FRUZAQLA。
• 对 FD&C Yellow 5 号(柠檬黄)和 6 号(日落黄 FCF)的过敏反应:含有 FD&C 黄色 5 号(柠檬黄)和 6 号(日落黄 FCF)作为色素添加剂,在某些易感患者中可能会引起过敏反应( 包括支气管哮喘)。
• 胚胎-胎儿毒性:可造成胎儿伤害。 告知有生殖潜力的患者对胎儿的潜在风险并使用有效的避孕措施。
【禁忌】
对本品任何成分过敏者禁用。
严重活动性出血、活动性消化道溃疡、未愈合的胃肠穿孔、消化道瘘患者禁用。重度肝
肾功能不全患者禁用。妊娠、哺乳期妇女禁用。
【特殊人群】
妊娠期:根据动物研究结果及其作用机制,本品给孕妇服用时可能会造成胎儿伤害。
哺乳期:建议女性在使用本品治疗期间以及最终剂量后至少2周内不要母乳喂养。
儿童:尚未确定本品对18岁以下患者的安全性和有效性。
老年患者: 与年轻患者相比,没有观察到老年患者在安全性或有效性方面的临床上重要的差异。
肝损伤患者:对于轻度肝功能不全(总胆红素小于或等于 ULN,AST 大于 ULN 或总胆红素大于 1 至 1.5 倍 ULN,伴任何 AST)的患者,不建议调整剂量。
FRUZAQLA 尚未在中度肝功能不全(总胆红素大于 1.5 倍并小于 3 倍 ULN 和任何 AST)患者中进行充分研究。 FRUZAQLA 不建议用于严重肝功能不全(总胆红素大于 ULN 3 倍和任何 AST)的患者。
【适应症】
本品单药适用于既往接受过氟尿嘧啶类、奥沙利铂和伊立替康为基础的化疗,以及既往接受过或不适合接受抗血管内皮生长因子(VEGF)治疗、抗表皮生长因子受体(EGFR)治疗(RAS野生型)的转移性结直肠癌(mCRC)患者。
【药物相互作用】
强或中度 CYP3A 诱导剂:避免同时使用。




 在线咨询
在线咨询 400-001-9769
400-001-9769
