【适应症】
本品是一种双特异性 HER2 和 HER3 抗体,适用于治疗:
1)患有晚期、不可切除或转移性非小细胞肺癌 (NSCLC) 的成人患者,该患者携带神经调节蛋白 1 (NRG1) 基因融合,并且在先前全身治疗期间或之后病情出现进展。
2) 患有晚期、不可切除或转移性胰腺腺癌的成人患者,该患者携带神经调节蛋白 1 (NRG1) 基因融合,并且在先前全身治疗期间或之后病情出现进展。
【推荐剂量】
-根据 NRG1 基因融合的存在情况选择接受 BIZENGRI 治疗的患者。
-在开始使用 BIZENGRI 之前评估左心室射血分数 (LVEF)。
-本品的推荐剂量为每 2 周一次,每次 750 mg,直至病情进展或出现不可接受的毒性。
-每次输液前均需使用治疗前用药,以降低输液相关反应的风险。
-稀释后以静脉输液方式给药,输液时间持续4 小时。
【不良反应】
-患者最常见的不良反应(≥ 10%):
腹泻、肌肉骨骼疼痛、疲劳、恶心、输液相关反应 、呼吸困难、皮疹、便秘、呕吐、腹痛和水肿。
-最常见的 3 级或 4 级实验室异常(≥ 2%):
GGT 升高、血红蛋白降低、钠降低、血小板减少、AST 升高、ALT 升高、碱性磷酸酶升高、镁降低、磷酸盐降低、aPTT 增加和胆红素升高。
【药理作用】
本品是一种双特异性抗体,可与细胞(包括肿瘤细胞)表面表达的 HER2 和 HER3 的胞外结构域结合,抑制 HER2:HER3 二聚化并阻止 NRG1 与 HER3 结合。本品通过磷酸肌醇 3-激酶 (PI3K)-AKT 哺乳动物雷帕霉素靶蛋白 (mTOR) 通路降低细胞增殖和信号传导。此外,本品介导抗体依赖性细胞毒作用 (ADCC)。本品在 NRG1 融合阳性肺癌和胰腺癌小鼠模型中表现出抗肿瘤活性。
【贮藏】
原包装盒内在冰箱中避光保存,温度为 2°C 至 8°C (36°F 至 46°F)。请勿冷冻。请勿摇晃。
【有效期】
18个月
【使用方法】
1. 患者选择
根据肿瘤标本中是否存在 NRG1 基因融合来选择接受本品治疗的患者。
2. 开始使用本品前建议进行评估
开始使用本品前,评估左心室射血分数 (LVEF)。
3.推荐剂量
-本品的推荐剂量为每 2 周静脉输注 750 mg,直至病情进展或出现不可接受的毒性。
-每次本品输注前均应按建议进行治疗前用药,以降低输注相关反应的风险。
4. 推荐的治疗前用药
每次输注本品之前,应进行治疗前用药以降低输液相关反应 (IRR) 的风险(见表 1)。
表 1:本品输注前的治疗前用药

1 初次 BIZENGRI治疗后可选
5. 准备
在给药前稀释并准备本品供静脉输注。对于初次输注,应尽可能在接近给药时间时准备本品,以便在发生输注相关反应时延长输注时间。
-检查本品溶液是否清澈至略带乳白色、无色至略带黄色。在溶液和容器允许的情况下,应在给药前目视检查肠外药物产品是否有颗粒物和变色。如果存在变色或可见颗粒,请勿使用。
-从 250 ml输液袋中取出并丢弃 37.5 ml 0.9% 氯化钠注射液。仅使用由聚氯乙烯 (PVC)、聚烯烃或聚烯烃/聚酰胺共挤塑料制成的输液袋。
-从 2 个小瓶中取出总共 37.5 ml 本品并将其添加到输液袋中。输液袋中的最终容量应为250 ml。丢弃小瓶中剩余的任何未使用部分。
-轻轻倒置袋子以混合溶液。不要摇晃。
-如果不立即使用,请将稀释溶液冷藏在 2°C 至 8°C温度下,并在制备后避光,除非在制备后 2 小时内开始输液。
6. 给药
-如果输液时间超过建议的储存时间,则必须丢弃输液袋并准备新的输液袋以继续输液。稀释的本品 溶液必须在以下时间内给药:
1) 输注溶液制备结束后储存在室温下 [15°C 至 25°C] 6 小时内
2)输注溶液制备结束后冷藏储存 [2°C 至 8°C] 28 小时内
-如果稀释的本品溶液已冷藏,请在给药前让其达到室温(约 30 分钟)。
-通过静脉输注给予稀释的本品溶液,使用由 PVC、聚乙烯 (PE)、聚氨酯 (PUR) 或聚丁二烯 (PB) 制成的输注器,并配有在线、无菌、无热原、低蛋白结合聚醚砜 (PES) 过滤器(孔径 0.2 微米)。
-请勿在同一静脉输液管中与其他药物同时输注本品。
-通过外周或中心静脉输液管输注本品。
-在本品输注期间密切监测患者是否出现输注相关反应的症状和体征,并在完成第一次本品输注后至少 1 小时内监测患者,并根据临床指证进行监测 。
-静脉输注时间持续 4 小时。
【剂量调整】
不良反应的剂量调整
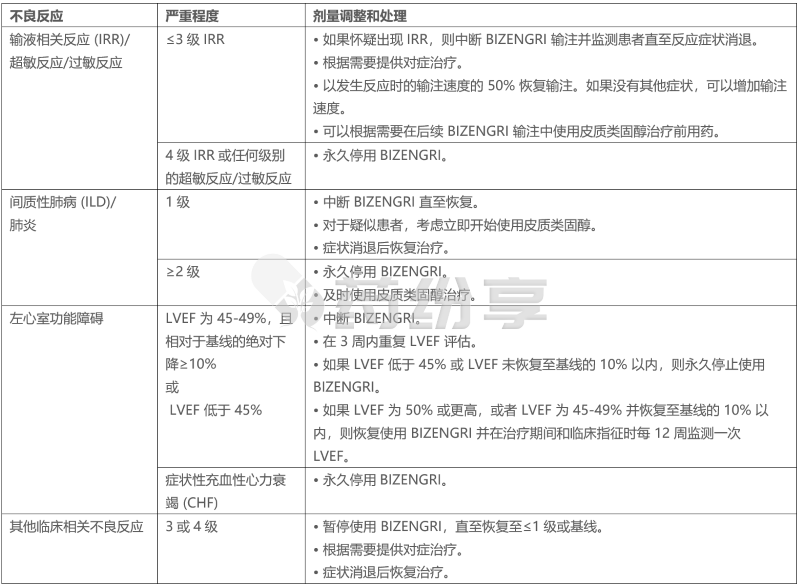
不建议减少本品的剂量。表 2 提供了针对不良反应的本品剂量调整建议。
表 2:针对不良反应的本品剂量调整和处理建议
【延迟或遗漏给药】
无相关信息
【过量处理】
无相关信息
【不良反应】
-患者最常见的不良反应(≥ 10%):
腹泻、肌肉骨骼疼痛、疲劳、恶心、输液相关反应 、呼吸困难、皮疹、便秘、呕吐、腹痛和水肿。
-最常见的 3 级或 4 级实验室异常(≥ 2%):
GGT 升高、血红蛋白降低、钠降低、血小板减少、AST 升高、ALT 升高、碱性磷酸酶升高、镁降低、磷酸盐降低、aPTT 增加和胆红素升高。
【注意事项】
-输液相关反应 (IRR)/超敏反应/过敏反应:
在配备紧急复苏设备和经过培训的工作人员的环境中使用本品,这些人员可以监测 IRR 并管理紧急药物。监测 IRR 的症状和体征。对于 IRR ≤ 3 级的患者,应中断输液并根据需要进行对症治疗。症状消退后,以较低的速度恢复输液。如果出现 4 级或危及生命的 IRR 或超敏反应/过敏反应,应立即停止输液并永久停用本品。
-间质性肺病 (ILD)/肺炎:
监测ILD/肺炎新的或恶化的肺部症状。对于 ≥ 2 级 ILD/肺炎的患者,永久停用本品。
-左心室功能障碍:
在开始使用本品之前以及在治疗期间根据临床指征定期评估 LVEF。通过中断或停止治疗进行处理理。对于症状性充血性心力衰竭 (CHF) 患者,永久停用本品。
-
【禁忌症】
无
【特殊人群】
-妊娠期:
根据其作用机制,本品给孕妇服用时可能会造成胎儿伤害。
-哺乳期:
没有关于本品是否存在于人乳中、对母乳喂养婴儿的影响或对产奶量的影响的数据。已知母体 IgG1 存在于人乳中。B本品对母乳喂养儿童的局部胃肠道暴露和有限的全身暴露的影响尚不清楚。考虑母乳喂养对发育和健康的益处,以及母亲对本品治疗的临床需求以及本品或潜在的母体疾病对母乳喂养儿童的任何潜在不利影响。这一考虑还应考虑到本品的消除半衰期和 2 个月的洗脱期。
-具有生育能力的女性和男性:
在开始本品之前验证女性的妊娠状况。建议有生育能力的女性患者在使用本品治疗期间以及最后一次服药后 2 个月内采取有效的避孕措施
-儿童:
尚未确定本品对儿童患者的安全性和有效性。
-老年患者与年轻患者相比,没有观察到≥65岁患者在安全性或有效性方面的临床上重要的差异。
【适应症】
本品是一种双特异性 HER2 和 HER3 抗体,适用于治疗:
1)患有晚期、不可切除或转移性非小细胞肺癌 (NSCLC) 的成人患者,该患者携带神经调节蛋白 1 (NRG1) 基因融合,并且在先前全身治疗期间或之后病情出现进展。
2) 患有晚期、不可切除或转移性胰腺腺癌的成人患者,该患者携带神经调节蛋白 1 (NRG1) 基因融合,并且在先前全身治疗期间或之后病情出现进展。
【药物相互作用】
无相关信息


 在线咨询
在线咨询 400-001-9769
400-001-9769
