【适应症】
本品适用于治疗正在服用氯巴占、年龄6个月及以上且体重≥7kg患者的Dravet 综合征 (DS) 相关癫痫发作。
尚无临床数据支持本品作为单药治疗Dravet 综合征。
【推荐剂量】
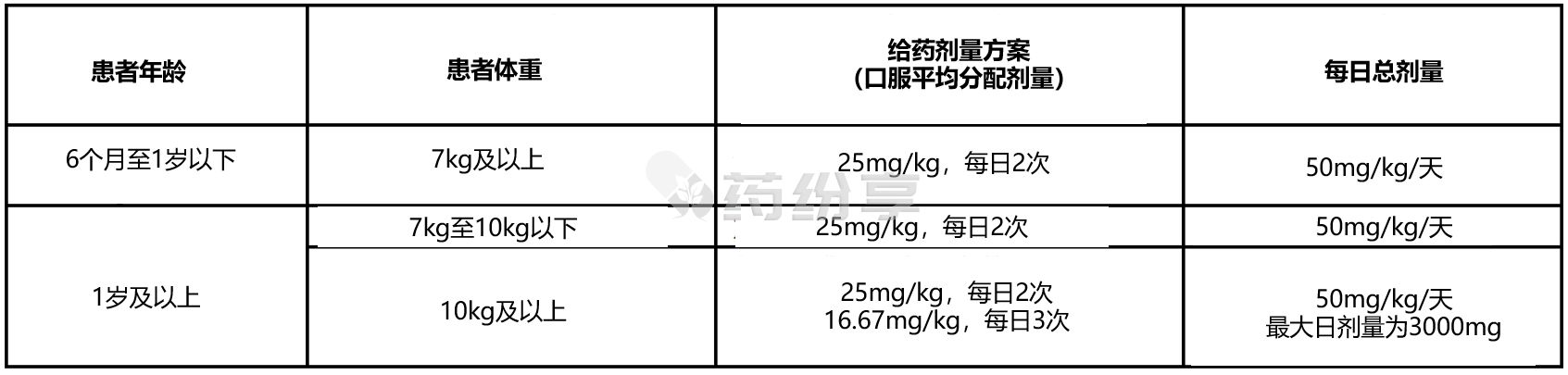
1、推荐口服剂量为50 mg/kg/天,分2或3次给药(即16.67 mg/kg,每日3次 或 25mg/kg,每日2次),具体取决于患者的年龄和体重(见下方表1)
2、如果无法达到确切剂量,则四舍五入至最接近的剂量,通常剂量范围为50mg-150mg。
3、最大推荐总剂量为3,000 mg/天。
【不良反应】
最常见的不良反应(至少10%):嗜睡,减少食欲不振、共济失调、体重减轻、肌张力减退、恶心、震颤、构音障碍和失眠。
【服用方法】
-本品口服用药
-本品胶囊需整粒吞服,与食物同服,切勿打开或破损
-如果您错过了一剂 ,请在您记得后立即服用。如果快到下一剂量服用预定的时间,请跳过错过的剂量,并在您的正常时间服用下一剂。切勿同时服用双倍剂量。
【推荐剂量】
1、推荐口服剂量为50 mg/kg/天,分2或3次给药(即16.67 mg/kg,每日3次 或 25mg/kg,每日2次),具体取决于患者的年龄和体重(见下方表1)
2、如果无法达到确切剂量,则四舍五入至最接近的剂量,通常剂量范围为50mg-150mg。
3、最大推荐总剂量为3,000 mg/天。

【服用方法】
-本品口服用药
-本品胶囊需整粒吞服,与食物同服,切勿打开或破损
-如果您错过了一剂 ,请在您记得后立即服用。如果快到下一剂量服用预定的时间,请跳过错过的剂量,并在您的正常时间服用下一剂。切勿同时服用双倍剂量。
【不良反应】
最常见的不良反应(至少10%):
1、嗜睡、食欲下降、激越、
2、共济失调、体重下降、张力减退
3、恶心、震颤、构音障碍 和失眠
【注意事项】
-嗜睡
本品可引起嗜睡。在 Dravet 综合征患者的对照研究中,本品治疗组患者的嗜睡发生率为67%,相比之下,安慰剂组患者的发生率为23%。两组中的所有患者均合并使用氯巴占,已知氯巴占也会引起嗜睡。本品与氯巴占联合给药导致氯巴占及其活性代谢物水平升高。其他中枢神经系统抑制剂(包括酒精)可增强本品的嗜睡作用。
处方医生应监测患者是否出现嗜睡。如果在与氯巴占同时给药期间发生嗜睡,考虑氯巴占初始剂量减少25%。如果嗜睡持续存在,应考虑进一步将氯巴占减少25%,并应调整其他具有镇静作用的合并抗惊厥药物的剂量。
处方医师应提醒患者不要从事需要精神警觉的危险活动,如操作危险机械或机动车,直至本品对精神警觉的影响已知。
-食欲下降和体重下降
本品可引起食欲和体重下降。在 Dravet 综合征患者的对照研究中,本品治疗患者中食欲下降的发生率为46%,相比之下,安慰剂组患者为10%。本品治疗组患者的体重下降发生率为27%,而安慰剂组患者为6%。接受本品治疗的患者中恶心和呕吐的发生率也更高。鉴于这些不良反应的频率,应仔细监测接受本品治疗的儿科患者的生长。在某些情况下,将合并使用的丙戊酸盐剂量减少30%/周可减少食欲和体重减轻。
-中性粒细胞减少症和血小板减少症
本品可引起中性粒细胞计数显著下降。在 Dravet 综合征患者的对照研究中,31例接受本品治疗的患者获得了基线和研究结束中性粒细胞计数。在这些接受本品治疗的患者中,有13%的患者在试验期间观察到中性粒细胞计数从基线时正常降低至低于1500个细胞/mm 3,但在任何安慰剂治疗的患者中均未观察到。
本品可引起血小板计数显著下降。在 Dravet 综合征患者的对照研究中,31例接受本品治疗的患者具有基线和研究结束血小板计数。在13%的本品治疗患者中观察到血小板计数从基线时正常降低至试验期间低于150,000/µL,但在任何安慰剂治疗患者中均未观察到。
应在开始本品治疗前进行血液学检查,然后每6个月进行一次。
-戒断症状
与大多数抗癫痫药物一样,本品通常应逐渐停药,以尽量减少癫痫发作频率增加和癫痫持续状态的风险。
在需要快速停用本品 的情况下(例如,在严重不良反应的情况下),建议进行适当监
-苯丙酮尿症患者的风险
苯丙氨酸对苯丙酮尿症 (PKU) 患者可能有害。本品口服混悬剂含有苯丙氨酸,一种阿斯巴甜成分。每个 250 mg 包装含1.40 mg苯丙氨酸;每 500 mg 包装含2.80 mg苯丙氨酸。在为 PKU 患者处方本品口服混悬剂之前,考虑所有来源的苯丙氨酸每日总量,包括本品口服混悬剂。
本品 胶囊不含苯丙氨酸。
-自杀行为和意念
AED(包括本品)会增加服用这些药物治疗任何适应症的患者自杀想法或行为的风险。接受任何 AED 治疗任何适应症的患者应监测抑郁的出现或恶化、自杀想法或行为和/或情绪或行为的任何异常变化。
任何考虑处方本品或任何其他 AED 的人必须平衡自杀想法或行为的风险与未治疗疾病的风险。癫痫和许多其他处方 AED 的疾病本身与发病率和死亡率以及自杀想法和行为风险增加相关。如果在治疗期间出现自杀想法和行为,处方医生需要考虑任何特定患者出现的这些症状是否与正在治疗的疾病有关。
应告知患者、其护理人员和家属 AED 会增加自杀想法和行为的风险,应告知其需要警惕抑郁体征和症状的出现或恶化、情绪或行为的任何异常变化或自杀想法、行为或自我伤害想法的出现。应立即向医疗保健提供者报告关注的行为。
【禁忌症】
无
【特殊人群】
怀孕:根据动物数据,可能会对胎儿造成伤害。
【适应症】
本品适用于治疗正在服用氯巴占、年龄6个月及以上且体重≥7kg患者的Dravet 综合征 (DS) 相关癫痫发作。
尚无临床数据支持本品作为单药治疗Dravet 综合征。
【药物相互作用】
-本品对其他药物的影响
CYP1A2、CYP2B6、CYP3A4、CYP2C8、CYP2C19、P-糖蛋白 (P-gp) 和乳腺癌耐药蛋白 (BCRP) 底物
体外数据显示,司替戊醇是CYP1A2、CYP2B6和 CYP3A4 的抑制剂和诱导剂。由于潜在的药物相互作用,当与本品伴随给药时,应根据临床情况考虑调整 CYP1A2 底物(如茶碱、咖啡因)、CYP2B6底物(如舍曲林、塞替派)和 CYP3A4 底物(如咪达唑仑、三唑仑、奎尼丁)的剂量。
由于可能抑制酶/转运蛋白活性,如果与本品伴随给药时发生不良反应,应考虑减少CYP2C8、CYP2C19底物(如地西泮、氯吡格雷)、P-gp底物(如卡马西平)和 BCRP 底物(如甲氨蝶呤、哌唑嗪、格列本脲)的剂量。
-氯巴占
本品(抑制 CYP 3A4 和2C19)与氯巴占合用导致氯巴占(CYP3A4的底物)和去甲氯巴占(氯巴占的活性代谢物,CYP2C19的底物)的血浆浓度升高。
这可能会增加氯巴占相关不良反应的风险。如果与本品联合给药时发生不良反应,考虑减少氯巴占的剂量。
-其他药物对本品的影响
当与CYP1A2、CYP3A4或 CYP2C19 强效诱导剂(如利福平、苯妥英、苯巴比妥和卡马西平)联合给药时,可能发生导致本品浓度降低的基于诱导的相互作用,因为这些酶均可代谢司替戊醇。
应避免本品与强诱导剂合并使用,或进行剂量调整。
-CNS 抑制剂和酒精
本品与其他 CNS 抑制剂(包括酒精)合并使用可能增加镇静和嗜睡的风险。
请按药品说明书或在药师指导下购买和使用





 在线咨询
在线咨询 400-001-9769
400-001-9769
