【适应症】
本品是一种蛋白酶体抑制剂,与来那度胺和地塞米松联合使用,用于治疗既往至少接受过一次治疗的多发性骨髓瘤患者。
【推荐用量】
-本品的推荐起始剂量: 在 28 天治疗周期的第 1、8 和 15 天,每周 1 次,每次口服给药 4 mg。
-来那度胺的推荐起始剂量: 在 28 天治疗周期的第 1-21 天,每日 1 次,每次给药 25 mg。
-地塞米松的推荐起始剂量: 在 28 天治疗周期的第 1、8、15 和 22 天给药,每次 40 mg。
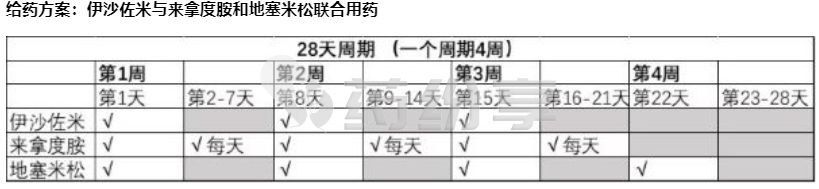
√=服用药物
关于来那度胺与地塞米松的更多信息,请参考来那度胺和地塞米松的药品说明书。
【不良反应】
最常见的不良反应(≥20%)为血小板减少、中性粒细胞减少、腹泻、便秘、周围神经病变、恶心、周围水肿、皮疹、呕吐和支气管炎。
【药理作用】
伊沙佐米是一种可逆性蛋白酶体抑制剂,可优先结合 20 S 蛋白酶体的β5 亚基并抑制其糜蛋白酶样活性。
伊沙佐米在体外可诱导多发性骨髓瘤细胞系凋亡,对经硼替佐米、来那度胺和地塞米松等多种药物治疗后复发患者的骨髓瘤细胞具有细胞毒作用,伊沙佐米和来那度胺合用对多发性骨髓瘤细胞系具有协同细胞毒作用。
伊沙佐米在小鼠多发性骨髓瘤异种移植模型中具有体内抗肿瘤活性。
【贮藏】
请勿冷冻,在 2~30°C 保存。为了防止受潮,请置于原包装中保存。
【有效期】
36个月
【使用方法】
本品需在具有多发性骨髓瘤治疗经验的医生的监督下开始治疗,并对治疗进行监测。
本品的给药途径为口服。
患者应该在每个治疗周期第 1、8 和 15 天大致相同的时间服药,在进餐前至少 1 小时或进餐后至少 2 小时服用本品。应用水送服整粒胶囊。请勿压碎、咀嚼或打开胶囊。
在开始一个新的治疗周期前:
中性粒细胞绝对计数应为 ≥ 1000/mm3
• 血小板计数应 ≥ 75, 000/mm3
• 根据医生判定,非血液学毒性一般应恢复至患者的基线状况或 ≤ 1 级 治疗应持续至疾病进展或出现不可接受的毒性。因为 24 个周期之后的耐受性和毒性相关数据有限,所以对于需要长于 24 个周期的联合给药治疗,应基于患者个体
获益风险评估结果。
【剂量调整】
剂量调整
表 1 列出了本品减量步骤,表 2 提供了剂量调整指南。
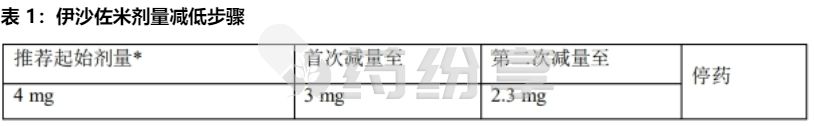
*患者伴有中度或重度肝损害、重度肾损害或需要透析的终末期肾病(ESRD)时,建议减量至 3 mg。
对于伊沙佐米和来那度胺血小板减少、中性粒细胞减少和皮疹的重叠毒性,建议交替调整伊沙佐米和来那度胺的剂量。对于这些毒性,剂量调整的第一步是停用/减低来那度胺剂量。
关于这些毒性的剂量减低步骤,参见来那度胺药品说明书。
表 2:伊沙佐米与来那度胺和地塞米松联用的剂量调整指南
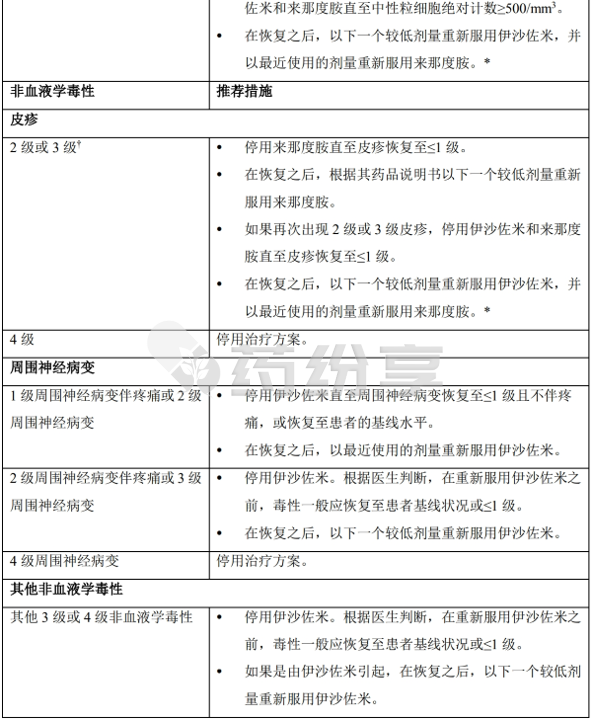
*如再次出现,交替调整来那度胺和伊沙佐米的剂量。
†根据美国国家癌症研究所通用术语标准(CTCAE)第 4.03 版进行分级。
合并用药
在接受本品治疗的患者中,应考虑抗病毒药物的预防治疗,降低带状疱疹病毒再激活的风险。在伊沙佐米研究中,接受抗病毒药物预防治疗患者的带状疱疹感染发生率低于未接受预防治疗的患者。
在接受本品联合来那度胺和地塞米松治疗的患者中,建议应该根据患者基础风险与临床状态的评估进行血栓预防治疗。
如果需要联合使用其他药品,请参考来那度胺与地塞米松的现行版药品说明书。
特殊患者人群
老年患者
对于年龄大于 65 岁的患者,无需调整本品的剂量。
在年龄大于 75 岁的患者中,伊沙佐米治疗方案组中有 13 例患者(28%),安慰剂治疗方案组中有 10 例患者(16%)报告停止治疗。在年龄大于 75 岁的患者中,伊沙佐米治疗方案组中有 10 例患者(21%),安慰剂治疗方案组中有 9 例患者(15%)出现心率失常。
肝损害
对于轻度肝损害患者(总胆红素≤正常值上限(ULN)和天冬氨酸转氨酶(AST)>ULN,或总胆红素>1-1.5×ULN 和 AST 任何水平),无需调整本品的剂量。对于中度(总胆红素>1.5-3×ULN)或重度(总胆红素>3×ULN)肝损害患者,建议减量至 3 mg。(见【药代动力
学】)
肾损害
对于轻度或中度肾损害患者(肌酐清除率≥30 mL/min),无需调整本品的剂量。对于重度肾损害(肌酐清除率<30mL/min)或需透析的终末期肾病(ESRD)患者,建议减量至 3mg。
伊沙佐米不能通过透析清除,因此给药时可以无需考虑透析时间(见【药代动力学】)。
肾损害患者的来那度胺给药建议,请参见其药品说明书。
儿童患者
尚未确定年龄小于 18 岁的儿科患者使用本品的安全性和疗效。尚无数据支持。
【延误或漏服剂量】
如果延误或漏服一剂本品,只有当距离下次计划给药时间 ≥ 72 小时,方可补服漏服剂量。距离在下次计划给药的 72 小时内不得补服漏服剂量。不得服用双倍剂量以弥补漏服的剂量。
如果患者在服药后呕吐,不应重复服药,而应在下次计划给药时恢复给药。
【药物过量】
尚无已知的用于伊沙佐米过量的特效解毒剂。虽然临床数据有限,但在随机化对照试验中已报告了剂量 ≤ 12 mg 的数据。如发生药物过量,应监测患者的不良反应并提供相应的支持性治疗。
【不良反应】
最常见的不良反应(≥20%)为血小板减少、中性粒细胞减少、腹泻、便秘、周围神经病变、恶心、周围水肿、皮疹、呕吐和支气管炎。
【注意事项】
-血小板减少症:
治疗期间至少每月监测一次血小板计数,并根据需要调整剂量。
-胃肠道毒性:
如果发生严重腹泻、便秘、恶心和呕吐,根据需要调整剂量。
-周围神经病变:
监测患者的周围神经病变症状,并根据需要调整剂量
-外周水肿:
监测液体潴留情况。适当时调查潜在原因。根据需要调整剂量。
-皮肤反应:
监测患者是否出现皮疹,并根据需要调整剂量。
-血栓性微血管病:
监测体征和症状。如果怀疑,请停用本品。
-肝毒性:
治疗期间监测肝酶。
-胚胎-胎儿毒性:
本品会对胎儿造成伤害。告知患者注意对胎儿的潜在风险,并使用有效的非激素避孕方法。
-在维持治疗中接受本品治疗的患者死亡率增加:
在试验之外,不建议在维持治疗中接受本品治疗多发性骨髓瘤患者。
【禁忌】
对本品活性成份或任何辅料过敏。
由于本品与来那度胺和地塞米松联合给药,所以关于禁忌方面的其他信息,请参考来那度胺和地塞米松的药品说明书。
【特殊人群】
-妊娠期:
根据其作用机制和动物繁殖研究的数据,本品给孕妇服用时会对胎儿造成伤害。
-哺乳期:
建议女性在本品治疗期间以及最后一次给药后90天内不要母乳喂养。
-儿童:
儿童患者的安全性和有效性尚未确定。
-老年患者:
在本品临床研究的受试者总数中,55%为65岁及以上,17%为75岁及以上。在这些受试者和年轻受试者之间没有观察到安全性或有效性的总体差异,其他报告的临床经验也没有发现老年人和年轻患者之间反应的差异,但不能排除一些老年人更敏感的可能性。
-肝损伤患者:
在中度或重度肝损伤患者中,与肝功能正常的患者相比,平均AUC增加了20%。减少中度或重度肝损伤患者的本品起始剂量。
-肾损伤患者:
在严重肾损伤或需要透析的ESRD患者中,与肾功能正常的患者相比,平均AUC增加了39%。在严重肾损伤或需要透析的ESRD患者中,减少本品的起始剂量。本品不会被透析移出,因此给药可以不考虑透析时间。
【适应症】
本品是一种蛋白酶体抑制剂,与来那度胺和地塞米松联合使用,用于治疗既往至少接受过一次治疗的多发性骨髓瘤患者。
【药物相互作用】
强效CYP3A诱导剂:避免与本品同时使用。
请按药品说明书或在药师指导下购买和使用







 在线咨询
在线咨询 400-001-9769
400-001-9769
