【适应症】
本品是一种靶向甲状腺素运载蛋白的小干扰核糖核酸(RNA),用于治疗成人遗传性转甲状腺素介导(hATTR)淀粉样变性的多发性神经病变。
【推荐剂量】
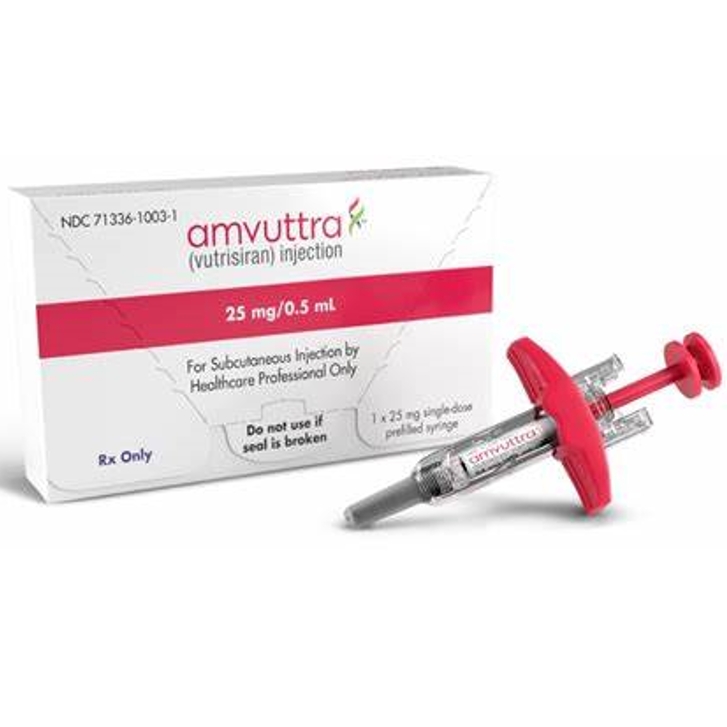
推荐剂量为每次25mg,皮下注射,每3个月给药一次。
【不良反应】
最常见的不良反应(≥5%):四肢疼痛,关节痛、呼吸困难和维生素A减少。
【药理作用】
本品是一种双链siRNA-GalNAc结合物,通过RNA干扰使突变型和野生型TTR Mrna降解,从而使血清TTR蛋白和TTR蛋白在组织中的沉积减少。
【贮藏】
-在2°C-30°C温度下保存,原包装未开封保存,直至使用。
-切勿冷冻
【有效期】
美版为24个月;欧盟版为3年
【使用方法】
-本品仅供皮下注射使用,并应由专业医护人员给药。
-给药前目视检查药液是否变色和有颗粒物。本品是一种无菌的、不含防腐剂的、透明的、无色至黄色的溶液。如果含有颗粒物质或混浊或变色,请勿使用。
-如果注射器储存在冷库中,在使用前让注射器升温至室温30分钟。
-本品注射的区域为:腹部、大腿或上臂。每次注射需要清洁所选注射部位。
-避免注射在肚脐周围5厘米的区域;疤痕组织或发红、发炎或肿胀的区域。
-不要重复使用注射器。
-使用过的注射器应立即丢弃。
【推荐剂量】
推荐剂量为每次25mg,皮下注射,每3个月给药一次。
【剂量调整】
无
【服用过量处理】
无
【漏服处理】
如果错过了一个剂量,请尽快补打。从最近一次用药开始,恢复每3个月用药周期。
【不良反应】
最常见的不良反应(≥5%):四肢疼痛,关节痛、呼吸困难和维生素A减少。
【注意事项】
-血清维生素A水平的降低和建议的补充措施:
本品治疗会导致血清维生素A水平下降。建议服用本品的病人按建议的每日维生素A摄入量进行补充。在使用本品治疗期间,不应给予比推荐的每日维生素A用量更高的剂量以试图达到正常的血清维生素A水平,因为血清维生素A水平并不能反映体内的总维生素A。如果患者出现提示维生素A缺乏的眼部症状(如夜盲症),应转诊到眼科医生就诊。
【禁忌】
无
【特殊人群】
-妊娠:
目前还没有关于孕妇使用本品的数据,以告知与本品相关的不良发育结果的风险。
-哺乳期:
目前还没有关于本品在母乳中的分泌、对哺乳期婴儿的影响或对乳汁分泌的影响的数据。
-儿童:
本品对儿科患者的安全性和有效性尚未确定。
-老年人:
对≥65岁的患者不需要调整剂量。在这些患者和年轻患者之间没有观察到安全性或有效性的总体差异,但不能排除一些老年人的更大敏感性。
-肾损伤:
轻度或中度肾脏损害(估计肾小球滤过率[eGFR]≥30至<90 mL/min/1.73 m²)的患者不建议调整剂量。本品尚未在严重肾功能损害或末期肾病患者中进行研究。
-肝损伤:
轻度肝功能损害(总胆红素≤1×ULN和AST>1×ULN,或总胆红素>1.0至1.5×ULN和任何AST)的患者不建议调整剂量。本品尚未在中度或重度肝功能损害患者中进行研究。
【适应症】
本品是一种靶向甲状腺素运载蛋白的小干扰核糖核酸(RNA),用于治疗成人遗传性转甲状腺素介导(hATTR)淀粉样变性的多发性神经病变。
【药物相互作用】
无相关数据。
请按药品说明书或在药师指导下购买和使用



 在线咨询
在线咨询 400-001-9769
400-001-9769
