【适应症】
本品是一种双特异性血管内皮生长因子 (VEGF) 和血管生成素-2 (Ang-2) 抑制剂,适用于治疗:
1、新生血管性(湿性)年龄相关性黄斑变性 (nAMD)
2、糖尿病性黄斑水肿(DME)
3、视网膜静脉阻塞继发性黄斑水肿 (RVO)
【推荐剂量】
-新生血管性(湿性)年龄相关性黄斑变性 (nAMD):
每次6mg(相当于0.05 ml),玻璃体内注射给药,初始前4个治疗剂量,每4 周一次(约每28天±7 天一次,每月一次),然后在完成第4次给药后的第8和第12周进行光学相干断层扫描(OCT)和视敏度评估,以确定是否需要按照以下三种方案之一继续给药,每次6mg,玻璃体内注射给药:1)第28和44周;2)第24、36、48周;或3)第20、28、36和44周。
尽管与每8周一次给药方案相比,按照每4周一次方案给药后在大多数患者中未见疗效提高,但在完成前4次给药后仍可能需要继续按照原来的每4周一次(每月一次)给药方案对一些患者进行治疗。应定期对患者进行评估。
-糖尿病性黄斑水肿:
推荐按照以下两种给药方案之一给药:
方案1:每次6mg(相当于0.05 ml),玻璃体内注射给药,每4周给药一次(约每28天±7 天一次,每月一次),持续给药至少4次。如果在至少4次给药后,根据光学相干断层扫描(OCT)测得的黄斑中心凹视网膜厚度(CST)确定水肿消退,可根据CST和视力评估结果调整给药间隔,如病情稳定,可延长给药间隔,每次延长不超过4周;如病情出现恶化,则应缩短给药间隔,每次缩短不超过8周。
方案2:每次6mg(相当于0.05 ml),玻璃体内注射给药,每4周给药一次,持续给药6次,随后每8周(2个月)给药一次,每次6mg。尽管与每8周一次给药方案相比,按照每4周一次方案给药后在大多数患者中未见疗效提高,但在完成前4次给药后仍可能需要继续按照原来的每4周一次(每月一次)给药方案对一些患者进行治疗。应定期对患者进行评估。
-视网膜静脉阻塞继发性黄斑水肿 (RVO)
推荐剂量为每次6mg(相当于0.05 ml),玻璃体内注射给药,每4周给药一次(约每28天±7 天一次,每月一次),持续6个月。
【不良反应】
-最常见的不良反应 (≥ 5%):白内障(15%)和结膜出血(8%)。
-最严重的不良反应为葡萄膜炎(0.6%)、感染性眼内炎(0.5%)、玻璃体炎(0.3%)、视网膜撕裂(0.2%)、孔源性视网膜脱离(0.1%)和外伤性白内障(<0.1%)。
【药理作用】
本品是一种人源化双特异性抗体,通过与VEGF-A和Ang-2结合而抑制两条通路发挥作用:通过抑制 VEGF-A,本品可抑制内皮细胞增殖、新生血管形成和血管通透性;通过抑制Ang-2,本品可提高血管稳定性并降低血管对VEGF-A的敏感性。在一些DME和nAMD患者中可见Ang-2水平升高,Ang-2 的抑制对DME和nAMD的治疗作用及临床应答的贡献尚待确定。
【贮藏】
在2°C-8°C温度下冷藏保存。
切勿冷冻,切勿摇晃。
放置于原包装盒内避光保存
【有效期】
30个月
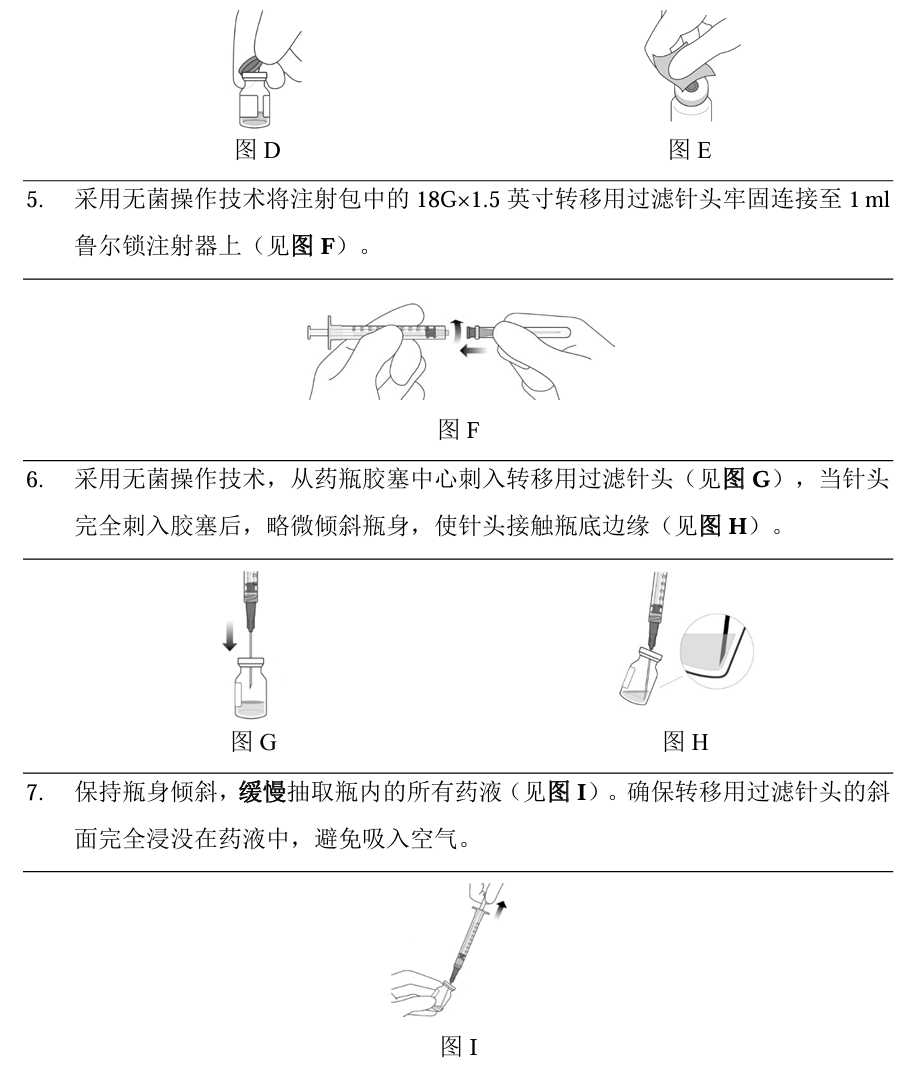
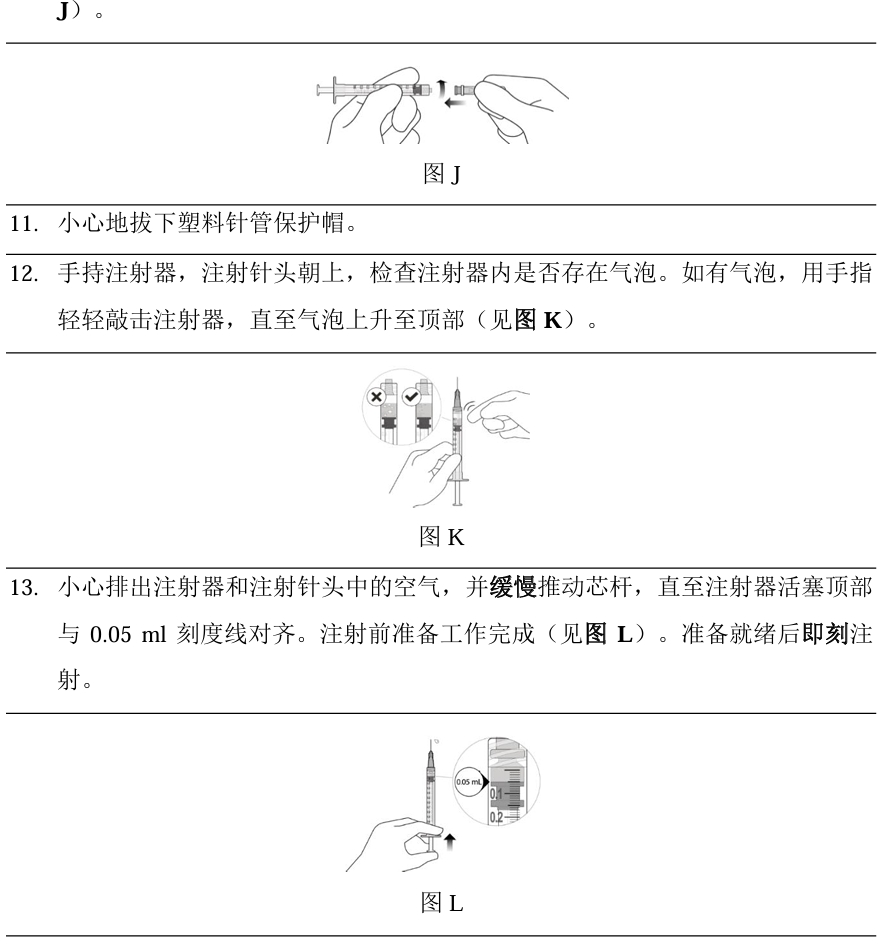
【使用方法】
-玻璃体内注射。本品应由具备资质的医生给药。每瓶药物仅供单眼治疗。
-给药前,本品应放置至20°C~25°C。本品在该温度下最长可放置24小时。
-给药前,应目视检查药液中是否存在微粒物和变色。本品为无色至棕黄色,且澄清至乳光溶液。 如有可见微粒物、浑浊或变色,切勿使用。 如果包装、药瓶和/或转移用过滤针头过期、损坏或遭窃启,切勿使用。


【推荐剂量】
-新生血管性(湿性)年龄相关性黄斑变性 (nAMD):
每次6mg(相当于0.05 ml),玻璃体内注射给药,初始前4个治疗剂量,每4 周一次(约每28天±7 天一次,每月一次),然后在完成第4次给药后的第8和第12周进行光学相干断层扫描(OCT)和视敏度评估,以确定是否需要按照以下三种方案之一继续给药,每次6mg,玻璃体内注射给药:1)第28和44周;2)第24、36、48周;或3)第20、28、36和44周。
尽管与每8周一次给药方案相比,按照每4周一次方案给药后在大多数患者中未见疗效提高,但在完成前4次给药后仍可能需要继续按照原来的每4周一次(每月一次)给药方案对一些患者进行治疗。应定期对患者进行评估。
-糖尿病性黄斑水肿:
推荐按照以下两种给药方案之一给药:
方案1:每次6mg(相当于0.05 ml),玻璃体内注射给药,每4周给药一次(约每28天±7 天一次,每月一次),持续给药至少4次。如果在至少4次给药后,根据光学相干断层扫描(OCT)测得的黄斑中心凹视网膜厚度(CST)确定水肿消退,可根据CST和视力评估结果调整给药间隔,如病情稳定,可延长给药间隔,每次延长不超过4周;如病情出现恶化,则应缩短给药间隔,每次缩短不超过8周。
方案2:每次6mg(相当于0.05 ml),玻璃体内注射给药,每4周给药一次,持续给药6次,随后每8周(2个月)给药一次,每次6mg。尽管与每8周一次给药方案相比,按照每4周一次方案给药后在大多数患者中未见疗效提高,但在完成前4次给药后仍可能需要继续按照原来的每4周一次(每月一次)给药方案对一些患者进行治疗。应定期对患者进行评估。
-视网膜静脉阻塞继发性黄斑水肿 (RVO)
推荐剂量为每次6mg(相当于0.05 ml),玻璃体内注射给药,每4周给药一次(约每28天±7 天一次,每月一次),持续6个月。
【剂量调整】
不建议对本品进行剂量调整。
【服用过量处理】
无
【漏服处理】
如果延迟或错过给药,患者应在下次就诊时返院接受医生评估,并根据医生的判断决定是否继续给药。
如果视力和/或解剖学结果表明患者无法从继续治疗中获益,则应停用本品。
【不良反应】
-最常见的不良反应 (≥ 5%):白内障(15%)和结膜出血(8%)。
-最严重的不良反应为葡萄膜炎(0.6%)、感染性眼内炎(0.5%)、玻璃体炎(0.3%)、视网膜撕裂(0.2%)、孔源性视网膜脱离(0.1%)和外伤性白内障(<0.1%)。
【注意事项】
-眼内炎和视网膜脱离:
玻璃体内注射给药可能发生眼内炎和视网膜脱离。应指导患者及时告知任何提示眼内炎或视网膜脱离的症状,并及时采取相关医治措施。
-眼内压升高:
在包括使用本品在内的玻璃体内注射后,在60分钟内可能观察到眼内压(IOP)短暂升高。应适当监测和医治眼内压(IOP)
-血栓栓塞事件:
存在与VEGF抑制有关的动脉血栓栓塞事件 (ATE) 的潜在风险。
【禁忌】
-眼或眼周感染患者禁用本品。
-活性眼内炎症患者禁用本品。
-在已知对本品或其任何赋形剂过敏的患者中,禁用本品。
【特殊人群】
-儿童用药
尚未确立本品在儿童患者中的安全性和有效性。
-肾功能不全
尚未在肾功能不全患者中针对本品开展任何特定研究。对所有临床研究(其中64%的患者有肾功能损害[轻度38%、中度24%和重度2%])中的患者进行的药代动力学分析显示,本品璃体内给药后全身药代动力学无差异。肾功能不全患者无需调整本品的剂量。
-肝功能不全
尚未在肝功能不全患者中针对本品开展任何特定研究。但是,该人群用药无需特殊考虑,因为本品通过蛋白水解进行代谢,不依赖于肝功能。肝功能不全患者无需调整剂量。
【适应症】
本品是一种双特异性血管内皮生长因子 (VEGF) 和血管生成素-2 (Ang-2) 抑制剂,适用于治疗:
1、新生血管性(湿性)年龄相关性黄斑变性 (nAMD)
2、糖尿病性黄斑水肿(DME)
3、视网膜静脉阻塞继发性黄斑水肿 (RVO)
【药物相互作用】
尚未进行相容性研究,因此本品不得与其他药品混合使用。
请按药品说明书或在药师指导下购买和使用






 在线咨询
在线咨询 400-001-9769
400-001-9769
