- 相关文章
达拉非尼,作为BRAF抑制剂领域的佼佼者,自诞生以来便肩负着对抗特定癌症的重任,在全球抗癌舞台上扮演着愈发重要的角色。2025年,达拉非尼在临床应用、医保政策以及药物研发等多个维度都迎来了新的突破与变革。医保覆盖范围的持续扩大,让更多患者有机会触及这一救命药物;全球多中心临床试验数据的不断公布,进一步验证了其在不同癌症治疗中的卓越疗效;而耐药机制与新型联合疗法的探索,则为解决长期治疗难题提供了新的思路。
然而,在达拉非尼为患者带来希望的同时,也面临着诸多挑战。仿制药与原研药的质量与价格博弈、不良反应的管理、特殊人群的用药安全等问题,都亟待解决。本文将深入剖析达拉非尼在2025年的全球临床数据、政策动态以及患者用药实操指南,为读者呈现一个全面、立体的达拉非尼抗癌图景,助力患者在这场抗癌征程中走得更稳、更远。
一、政策与医保动态:全球药物可及性提升的里程碑
1. 2025年医保政策信息
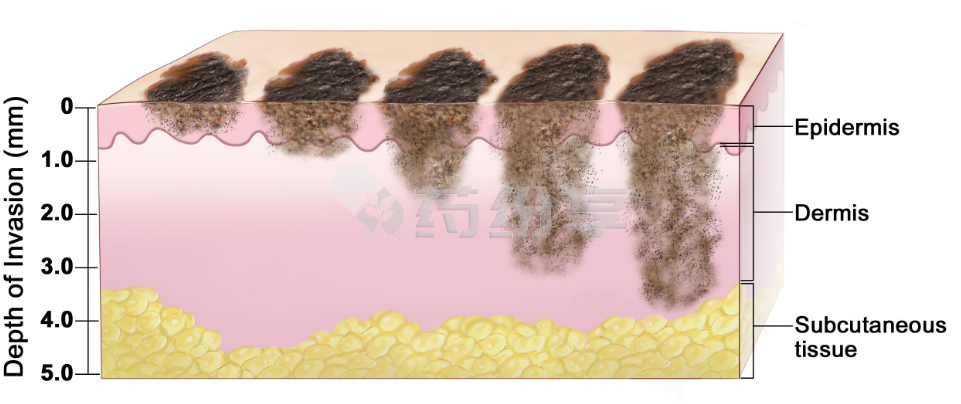
达拉非尼(Dabrafenib)作为诺华制药(Novartis)研发的BRAF抑制剂,其医保覆盖范围持续扩大。达拉非尼主要用于治疗携带有BRAF V600E或V600K突变的不可切除或转移性黑色素瘤、转移性非小细胞肺癌和局部晚期或转移性甲状腺未分化癌。其医保报销的适应症包括:BRAF V600突变阳性不可切除或转移性黑色素瘤,联合曲美替尼适用于治疗此类患者;BRAF V600突变阳性黑色素瘤的术后辅助治疗,联合曲美替尼适用于BRAF V600突变阳性的Ⅲ期黑色素瘤患者完全切除后的辅助治疗;以及BRAF V600突变阳性的转移性非小细胞肺癌,联合曲美替尼适用于治疗此类患者。
2. 仿制药与原研药竞争格局:质量与价格的博弈
在仿制药与原研药的竞争格局中,质量与价格的博弈尤为显著。原研药研发成本高、周期长,通常需耗费数十亿美元和10 - 15年时间,凭借其创新性和高质量标准在市场上占据一定优势,价格也相对较高。而仿制药在原研药专利到期后,通过仿制其化学成分和药理作用生产,研发成本和周期大幅降低,价格通常只有原研药的10% - 30%甚至更低,提高了药品的可及性。各国药监机构对仿制药审批严格,通过一致性评价的仿制药成分上与原研药一致。在市场竞争中,原研药凭借品牌影响力仍有一定份额,而仿制药则以价格优势逐渐扩大市场。
3.达拉非尼相关价格
达拉非尼在国内已经上市且纳入医保,国内75mg*120粒的最新售价在九千多到一万多元,具体医保价格请咨询当地医院药房。老挝卫生部已批准达拉非尼仿制药上市,其药物成分与原研药的药物成分基本一致,最新价格在两千元。

二、临床研究进展:从单药到联合疗法的全球突破
1. 2025年全球临床数据发布:BRAF突变NSCLC治疗新标准
2025年1月,诺华发表了一项全球多中心Ⅲ期临床试验(CDRB436E2201)的长期随访数据。研究显示,达拉非尼联合曲美替尼治疗BRAF V600E突变NSCLC患者的5年总生存率(OS)达22%,中位无进展生存期(PFS)延长至14.6个月,较化疗组提升3倍。该研究还首次证实,联合疗法可显著降低脑转移风险,脑转移患者的中位OS从6个月延长至18个月。基于这一数据,FDA于2025年3月批准达拉非尼联合曲美替尼作为BRAF突变NSCLC的一线治疗方案,并纳入NCCN指南推荐。
2. 术后辅助治疗突破:高龄患者的长期生存案例
在黑色素瘤领域,达拉非尼联合曲美替尼的术后辅助治疗价值得到进一步验证。一项中国多中心Ⅱ期临床试验结果:73例BRAF V600E突变Ⅲ期黑色素瘤患者接受12个月联合治疗后,3年无复发生存率(RFS)达68%,显著高于单药组的42%。其中,一名73岁男性患者在术后辅助治疗后实现5年无病生存,成为全球最高龄的长期获益案例。该研究还发现,联合治疗可降低皮肤鳞癌发生率,从单药组的12%降至3%。
三、不良反应与用药管理:全球患者的安全性挑战
1. 常见不良反应应对指南:从皮肤毒性到代谢紊乱
达拉非尼的全球不良反应谱与国内数据基本一致,但欧美患者更关注长期用药的代谢风险。根据FDA不良事件报告系统(FAERS)2025年数据,发热(63%)、皮疹(58%)和掌跖红肿疼痛综合征(45%)仍是最常见的不良反应。值得注意的是,欧美患者中高血糖发生率显著高于亚洲人群(28% vs. 15%),可能与饮食结构差异有关。美国FDA建议,糖尿病患者需每2周监测血糖,并避免联用CYP3A4强抑制剂(如酮康唑),以免血药浓度飙升引发酮症酸中毒。
2. 严重不良反应预警:新发恶性肿瘤与心脏毒性
达拉非尼的长期安全性问题仍是全球关注焦点。2025年,EMA提示达拉非尼可能增加新发恶性肿瘤风险,尤其是皮肤鳞癌(年发生率3%-5%)和结肠腺瘤(年发生率2%)。建议患者在治疗期间每2个月进行皮肤镜筛查,并每年接受结肠镜检查。此外,联合曲美替尼可能引发左心室射血分数(LVEF)下降,FDA要求患者治疗前需评估基线心功能,并在用药后每3个月复查超声心动图。
四、患者用药实操指南:从剂量调整到全球购药策略
1. 漏服、空腹服用与药物相互作用:全球患者的高频问题
达拉非尼的全球说明书明确指出,漏服剂量≥6小时需补服,否则跳过;强调餐前1小时或餐后2小时服药可提升生物利用度。在药物相互作用方面,FDA警告,达拉非尼与华法林联用可能增加出血风险,需将INR监测频率从每周1次提升至每周2次。此外,欧美患者常使用的圣约翰草可能降低达拉非尼血药浓度,需避免联用。
2. 特殊人群用药:全球共识与争议
在育龄女性中,FDA与EMA均要求停药后16周采取避孕措施,但印度药品监管局(DCGI)仅要求12周,引发争议。在儿童患者中,达拉非尼的全球剂量调整方案趋于统一:1岁以上儿童按体重计算剂量(4.5 mg/kg/次,每日2次),但需警惕生长发育迟缓风险。对于肝功能不全患者,FDA建议轻中度损伤者无需调整剂量,但重度损伤者禁用。

五、未来展望:耐药机制与新型联合疗法的全球探索
1. 耐药难题:从MAPK通路旁路激活到联合疗法突破
达拉非尼的耐药机制仍是全球研究热点。一项研究揭示,BRAF V600E突变NSCLC患者耐药后,约40%出现MAPK通路旁路激活(如MEK扩增或NRAS突变)。针对这一难题,诺华启动了全球Ⅲ期临床试验(COMBI-i),评估达拉非尼联合PD-1抑制剂斯巴达珠单抗(Spartalizumab)的疗效。初步数据显示,联合疗法可使耐药患者的客观缓解率(ORR)提升至35%,中位PFS延长至9个月。
2. 新适应症拓展:从低级别胶质瘤到罕见肿瘤
达拉非尼在新适应症上的探索取得突破。2025年,FDA批准达拉非尼联合曲美替尼用于治疗BRAF V600E突变的儿童低级别胶质瘤(pLGG),基于Ⅱ期临床试验(NCT02684058)的ORR达46%。在罕见肿瘤领域,达拉非尼单药治疗BRAF V600E突变的甲状腺未分化癌(ATC)的ORR达29%,中位OS延长至7.2个月,成为无满意局部治疗方案患者的最后希望。
结语:全球抗癌征程中的达拉非尼
从2013年FDA首次批准达拉非尼治疗黑色素瘤,到2025年成为BRAF突变NSCLC的一线治疗药物,达拉非尼的全球抗癌征程见证了精准医疗的崛起。未来,随着联合疗法与耐药机制研究的深入,达拉非尼有望为更多癌症患者带来生存希望。
参考资料:
1、https://www.ema.europa.eu/en/medicines/human/EPAR/tafinlar
2、https://clinicaltrials.gov/search?cond=Dabrafenib&viewType=Table
3、https://www.fda.gov/search?s=tafinlar
4、https://www.ema.europa.eu/en/documents/rmp/finlee-epar-risk-management-plan_en.pdf
5、https://www.mycancergenome.org/content/clinical_trials/NCT02684058/


