- 相关文章
2022年2月,美国FDA接受了adagrasib的新药申请(NDA ),用于治疗以前治疗过KRAS的患者G12C–非小细胞肺癌阳性。2022年12月,美国FDA批准加速批准adagrasib治疗KRASG12C-突变的局部晚期或转移性NSCLC,其先前已接受至少一种全身性治疗。Adagrasib加入索托拉西作为另一个KRAS G12CFDA批准的抑制剂。
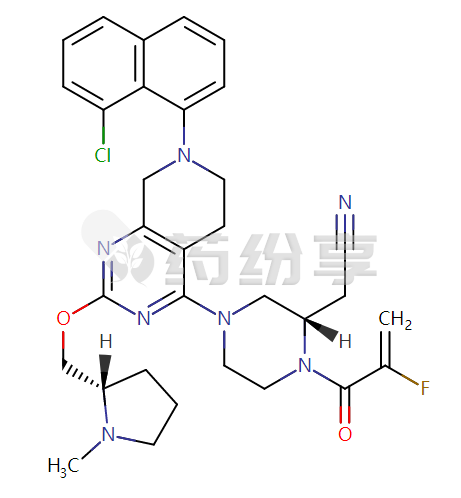
Adagrasib是一种KRAS抑制剂,用于治疗至少接受过一次全身治疗的局部晚期或转移性KRAS G12C突变非小细胞肺癌患者。Adagrasib (MRTX849)是一种由Mirati Therapeutics开发的口服小分子KRAS抑制剂。
AdagrasibI会导致严重的胃肠的不良反应。在汇总的安全人群中,观察到的严重胃肠道不良反应为3.8%的胃肠道出血,包括0.8%的3级或4级,1.6%的胃肠道梗阻,包括1.4%的3级或4级,结肠炎在0.5%包括0.3%的三级、肠梗阻在0.5%,和狭窄在0.3%。此外,366名患者中有89%出现恶心、腹泻或呕吐,包括9%的3级患者。恶心、腹泻或呕吐导致29%的患者剂量中断或剂量减少,0.3%的患者永久停用Adagrasib。使用监控和管理患者支持性护理,包括止泻药、止吐药或根据指示更换液体。根据严重程度暂停、减少剂量或永久停用Adagrasib。
Adagrasib可导致QTc间期延长,从而增加心室的快速性心律失常(如尖端扭转型室性心动过速)或猝死。在汇总的安全人群中,366名患者中有6%至少有一次基线后心电图(心电图)评估的平均QTc ≥ 501毫秒,11%的患者QTc较基线增加> 60毫秒。Adagrasib导致QTc间期的浓度依赖性增加。避免将Adagrasib与其他已知可能会延长QTc间期的药物同时使用。以下患者应避免使用Adagrasib天生的 长QT综合征和伴有QTc延长的患者。在开始使用Adagrasib之前、合并使用期间以及根据临床指征,对以下患者监测心电图和电解质充血性心力衰竭缓慢性心律失常,电解质异常,以及无法避免已知会延长QT间期的合并用药的患者。根据严重程度,暂停、减少剂量或永久停用Adagrasib参。
Adagrasib可引起肝毒性,这可能导致药物性肝损伤和肝炎。在366名患者的汇总安全性人群中,0.3%的患者报告了药物性肝损伤,其中0.3%为3级。总共有32%接受阿达格列西的患者病情有所增加丙氨酸转氨酶(备选)/增加天冬氨酸转氨酶(AST);5%为三级,0.5%为四级。首次出现ALT/AST升高的中位时间为3周(范围:0.1至48)。总体肝毒性发生率为37%,7%为3级或4级。12%的患者出现导致剂量中断或减少的肝毒性。0.5%的患者因肝毒性而停用Adagrasib。在开始服用KRAZATI前监测肝脏实验室检查(AST、ALT、碱性磷酸酶和总胆红素),连续3个月每月监测一次,或根据临床指示进行监测,对出现转氨酶升高的患者进行更频繁的检查。根据严重程度减少剂量、停止用药或永久停用Adagrasib。
Adagrasib可以导致间质性肺病(ILD)/肺炎,这可能是致命的。在汇总的安全人群中,4.1%的患者出现ILD/肺炎,1.4%为3级或4级,一例死亡。首次出现ILD/肺炎的中位时间为12周(范围:5至31周)。0.8%的患者因ILD/肺炎而停用Adagrasib。监测患者是否出现新的或恶化的指示ILD/肺炎的呼吸道症状(例如,气短在用KRAZATI治疗期间,咳嗽、发烧。对疑似ILD/肺炎的患者停用Adagrasib,如果未发现其他潜在的ILD/肺炎原因,则永久停用Adagrasib。
由于Adagrasib刚刚在海外上市不久,所以目前还比较难购买,想了解更多关于Adagrasib方面的信息可以咨询我们。


